Nedbrydningen af ozonlaget | VG3
Projecter »
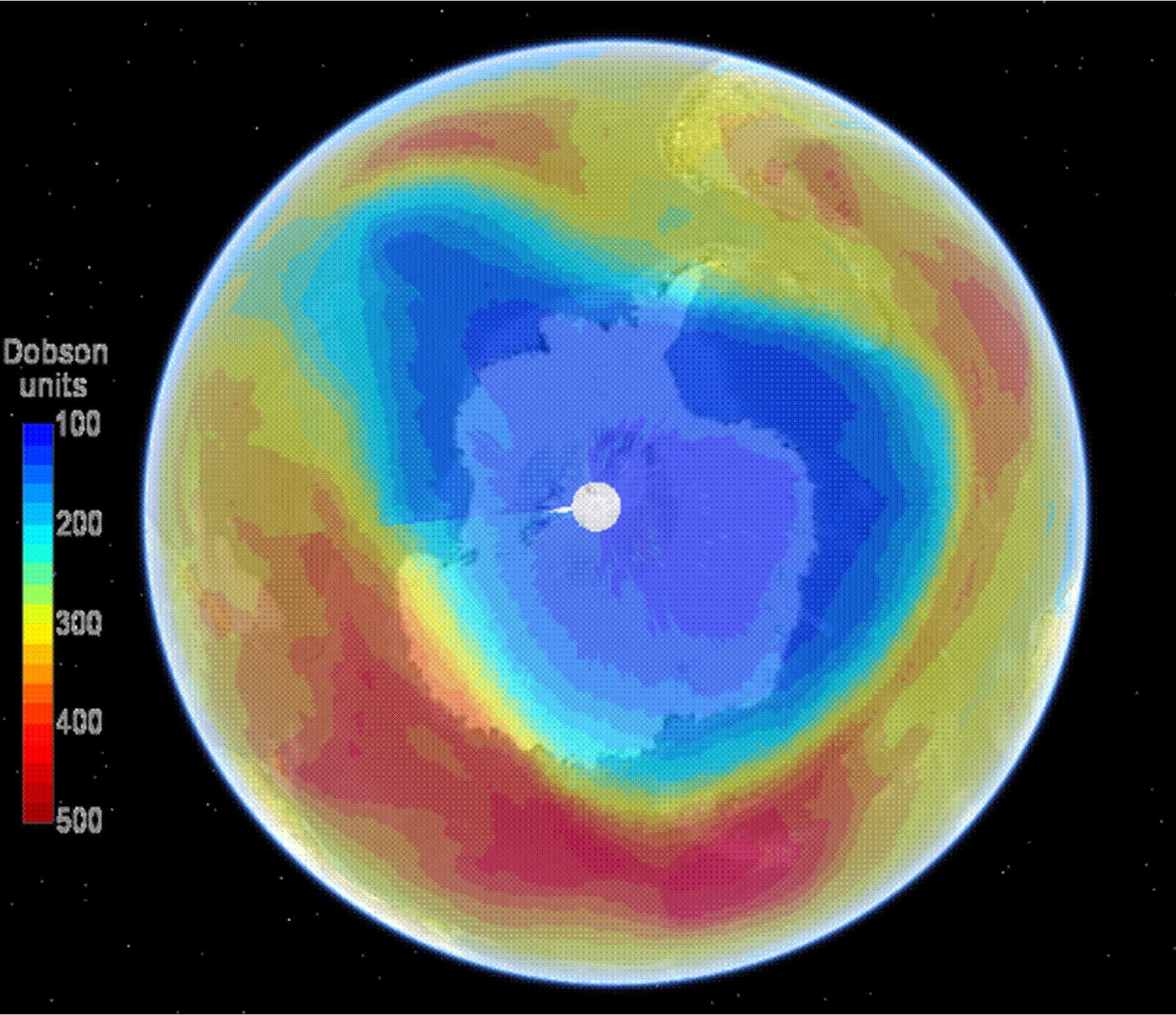
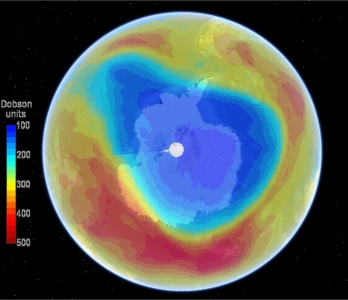
Først midt i 1980’erne fandt man ud af den rette sammenhæng:
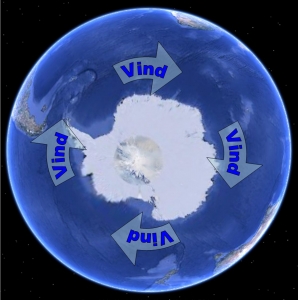
Temperaturforskellen mellem det Antarktiske fastlandsklima og havene omkring kontinentet skaber kraftige hvirvelvinde. Når ozonhullet især opstår over Antarktis, skyldes det netop de polare hvirvelvinde, for de blæser luft – med CFC – ind mod kontinentet. Ved Nordpolen er disse vinde ikke nær så stærke som ved Sydpolen.
Ozonhullet opstår hurtigt om foråret. Her er der utroligt koldt – under minus 80 °C, fordi Solen har været væk hele vinteren (som jo er i april-september på den sydlige halvkugle). Og fordi der er så koldt om foråret, samles skyer af små og kolde iskrystaller i stratosfæren over Antarktis. CFC-molekyler sætter sig på overfladen af iskrystallerne. Og når Solens første stråler kommer frem om foråret, rammes de CFC-molekyler, der sidder på iskrystallerne.
CFC står for Chloro-Fluoro-Carbon, det er altså en gruppe af kemiske forbindelser, der består af klor (se http://da.wikipedia.org/wiki/Klor), fluor (se http://da.wikipedia.org/wiki/Fluor), og kulstof (se http://da.wikipedia.org/wiki/Carbon). Når Solens stråler bager, så frigives klor-atomer fra CFC.

Fra http://infolink2003.elbo.dk/Naturvidenskab/dokumenter/doc/8465.pdf
Nedbrydning af ozon vist i powerpoint - klik!
1. Ultraviolet stråling rammer et CFC-molekyle og fraspaltger et kloratom.
Det sker primært, når Solen bryder frem om foråret over Antarktis. I løbet af den iskolde vinter sætter CFC-molekylerne sig fast på iskrystaller i de meget kolde stratosfæriske skyer. Når det første lys om foråret rammer iskrystallerne med CFC-molekylerne, fraspaltes klor.
2. Kloratomet bevæger sig med vinden rundt i stratosfæren. Før eller siden vil kloratomet i ozonlaget møde et ozonmolekyle.
3. I ozonlaget vil det enlige kloratom gå i forbindelse med det ene oxygenatom i ozonmolekylet, så ozonen nedbrydes og der dannes almindelig oxygen og klormonooxid:
O3 + Cl -> ClO + O2.
4. Klormonooxid er ikke nogen særlig stabil forbindelse, så når det støder på et oxygenatom dannes et oxygenmolekyle, der er en mere stabil forbindelse. ClO + O -> Cl + O2. Det enlige oxygenatom ville ellers have dannet ozon sammen med et oxygenmolekyle.
5. Der er nu igen et ledigt kloratom, og processen starter forfra (fra punkt 2). På denne måde kan et enkelt kloratom nå at ødelægge mange tusinde ozonmolekyler.
Andre animationer af ozonlagets funktion og nedbrydning:
http://www.bom.gov.au/lam/Students_Teachers/ozanim/ozoanim.shtml
http://svs.gsfc.nasa.gov/vis/a000000/a000800/a000825/index.html